Способы защиты от коррозии
Разработки в сфере коррозионной протекции
Рассмотрев, какие виды коррозии существуют, стоит описать, бывают ли орудия против них. Исследования в области защиты от коррозионных процессов проводятся на постоянной основе. На сегодняшний день самыми популярными методами борьбы против разрушителя металлической поверхности являются:
- Защитное покрытие.
- Воздействие на коррозионную среду с понижением активности среды (лишение коррозионной среды кислорода, использование ингибиторов процесса).
- Протекция электрохимического направления.
- Инновационная разработка и внедрение в производство новейших структурных материалов с повышенной устойчивостью к процессу разрушения. Суть метода заключается в вычленении из металлических сплавов добавок, которые катализируют разрушительный процесс (например, удаление из сплавов алюминия примеси железа, из сплавов железа – серы), либо прямопротивоположном процессе – внедрении в существующий сплав дополнительных элементов, передающих свою коррозионную устойчивость всему сплаву(к примеру, добавление хрома или никеля в сплав железа, усиление магниевых сплавов марганцем и т.п.).
- Использование в строительстве неметаллических компонентов, где это представляется возможным (высокополимерного пластика, стекла и керамики).
- Минимизация воздействия неблагоприятных условий на металл (отделение металлических конструкций от внешней среды, скорейший ремонт на участках скопления воды, удаление прощелин в цельных конструкциях).
Защитная пленка как преграда разрушению
Коррозия металлов не может проникнуть внутрь металлического изделия без внешних повреждений. На конструкции наносят покрытия – это и служит как специфическая защита. Ряд металлов известны нам по своей ценности в сфере ювелирного дела, так подобные пленки выполняют не только защитную функцию, но и эстетическую.
Металлические покрытия в свою очередь делятся на анодные и катодные. Анодные пленки выполняются из металла активнее, нежели внутренний защищаемый сплав. Катодные же, наоборот, выполнены из металла менее активного, и не направлены на протекцию нижнего слоя металл в случае видимых повреждений.
Неметаллические пленки так же разделены на 2 подвида: неорганические (эмали) и органические (лаки, краски, резина, битум).
Водородное охрупчивание
Атомы водорода проникают в структуру металлов, делая их хрупкими. Все подверженные водородному охрупчиванию материалы также крайне уязвимы для коррозионного растрескивания под напряжением.
Причины образования
Растрескивание под воздействием водорода может происходить, когда металл подвергается статическому или циклическому растягивающему напряжению. Водород может вызвать изменения механических свойств и поведения металла, в том числе:
- снижение пластичности (относительное удлинение и уменьшение площади);
- снижение ударной прочности и вязкости;
- усиление усталостных харатеристик.
Предотвратить водородное охрупчивание можно путем подбора стойких к воздействию водорода материалов, таких как аустенитные сплавы с содержанием никеля от 10 до 30 %.
Виды коррозии металлов
На сегодняшний день разновидностей коррозии металлов достаточно много, так как источниками её возникновения может выступать довольно большое количество разнообразных факторов. В целом коррозийные процессы классифицируют по нескольких параметров, а определённые типы коррозии различают между собой по схожести признаков проявления.
В зависимости от общего характера протекания коррозия может проявляться в двух основных формах, которые можно встретить и в повседневной жизни.
-
Общего характера — иными словами, её ещё называют равномерной. Эта разновидность является одной из самых распространённых, так как причинами её появления являются химические и электрохимические реакции. Общая может приводить к ухудшению всей поверхности предмета. Однако, несмотря на это, она является одной из самых безопасных, среди всех существующих. Связанна эта особенность, прежде всего, с тем, что такой процесс можно как предсказать, так и угадать. В этом случае коррозия может быть:
- равномерной — в этом случае ржа даёт о себе знать одновременно на всей поражённой территории. Примером может быть разрушение труб, изготовленных из железа, которые находятся на открытом воздухе;
- неравномерной — при этой разновидности скорость реакции разрушения на поверхности варьируется, то есть разрушения одного участка может происходить значительно быстрее, нежели, например, соседнего.
- Местного характера — в отличие от предыдущего эта разновидность ориентирована на одну конкретную область, на которой и возникает поражение.
Виды коррозии
Как уже говорилось, критериев классификация коррозионных процессов существует множество. Так, различают коррозию по виду распространения (сплошная, местная), по типу коррозионной среды (газовая, атмосферная, жидкостная, почвенная), по характеру механических воздействий (коррозионное растрескивание, явление Фреттинга, кавитационная коррозия) и так далее.
Но основным способом классификации коррозии, позволяющим наиболее полно объяснить все тонкости этого процесса, является классификация по механизму протекания.
По этому критерию различают два вида коррозии:
- химическую
- электрохимическую
Химическая коррозия
Химическая коррозия отличается от электрохимической тем, что протекает в средах, не проводящих электрический ток. Поэтому при такой коррозии разрушение металла не сопровождается возникновением электрического тока в системе. Это обычное окислительно-восстановительное взаимодействие металла с окружающей средой.
Наиболее типичным примером химической коррозии является газовая коррозия. Газовую коррозию еще называют высокотемпературной, поскольку обычно она протекает при повышенных температурах, когда возможность конденсации влаги на поверхности металла полностью исключена. К такому виду коррозии можно отнести, например, коррозию элементов электронагревателей или сопел ракетных двигателей.
Скорость химической коррозии зависит от температуры — при ее повышении коррозия ускоряется. Из-за этого, например, в процессе производства металлического проката, во все стороны от раскаленной массы разлетаются огненные брызги. Это с поверхности металла скалываются частички окалины.
Окалина — типичный продукт химической коррозии, — оксид, возникающий в результате взаимодействия раскаленного металла с кислородом воздуха.
Помимо кислорода и другие газы могут обладать сильными агрессивными свойствами по отношению к металлам. К таким газам относятся диоксид серы, фтор, хлор, сероводород. Так, например, алюминий и его сплавы, а также стали с высоким содержанием хрома (нержавеющие стали) устойчивы в атмосфере, которая содержит в качестве основного агрессивного агента кислород. Но картина кардинально меняется, если в атмосфере присутствует хлор.
В документации к некоторым антикоррозионным препаратам химическую коррозию иногда называют «сухой», а электрохимическую — «мокрой». Однако химическая коррозия может протекать и в жидкостях. Только в отличие от электрохимической коррозии эти жидкости — неэлектролиты (т.е. не проводящие электрический ток, например спирт, бензол, бензин, керосин).
Примером такой коррозии является коррозия железных деталей двигателя автомобиля. Присутствующая в бензине в качестве примесей сера взаимодействует с поверхностью детали, образуя сульфид железа. Сульфид железа очень хрупок и легко отслаивается, освобождая свежую поверхность для дальнейшего взаимодействия с серой. И так, слой за слоем, деталь постепенно разрушается.
Электрохимическая коррозия
Если химическая коррозия представляет собой не что иное, как простое окисление металла, то электрохимическая — это разрушение за счет гальванических процессов.
В отличие от химической, электрохимическая коррозия протекает в средах с хорошей электропроводностью и сопровождается возникновением тока. Для «запуска» электрохимической коррозии необходимы два условия: гальваническая пара и электролит.
В роли электролита выступает влага на поверхности металла (конденсат, дождевая вода и т.д.). Что такое гальваническая пара? Чтобы понять это, вернемся к ряду активности металлов.
Смотрим. Cлева расположены более активные металлы, справа — менее активные.
Если в контакт вступают два металла с различной активностью, они образуют гальваническую пару, и в присутствии электролита между ними возникает поток электронов, перетекающих от анодных участков к катодным. При этом более активный металл, являющийся анодом гальванопары, начинает корродировать, в то время как менее активный коррозии не подвергается.
Схема гальванического элемента
Для наглядности рассмотрим несколько простых примеров.
Допустим, стальной болт закреплен медной гайкой. Что будет корродировать, железо или медь? Смотрим в ряд активности. Железо более активно (стоит левее), а значит именно оно будет разрушаться в месте соединения.
Стальной болт — медная гайка (корродирует сталь)
А если гайка алюминиевая? Снова смотрим в ряд активности. Здесь картина меняется: уже алюминий (Al), как более активный металл, будет терять электроны и разрушаться.
Таким образом, контакт более активного «левого» металла с менее активным «правым» усиливает коррозию первого.
Рекомендации
Советы:
- На защите деталей лучше не экономить, и покрыть их резиновой или полимерной краской.
- Перед использованием абразивов нужно попробовать удалить ржавчину щадящими составами.
- Сложные коррозионные процессы можно останавливать с помощью агрессивных химикатов, но прежде чем их использовать, нужно изучить свойства состава, характеристики металла, чтобы предотвратить возможные негативные реакции.
Коррозионные процессы могут быстро разрушить любой материал. Порча металлоконструкций в некоторых ситуациях может иметь катастрофические последствия. Изучив способы защиты от образования коррозии, нужно применить один из наиболее подходящих.
ОСНОВНЫЕ ВИДЫ КОРРОЗИИ
Коррозией металлов называется их разрушение вследствие химического или электрохимического взаимодействия с окружающей средой. По механизму протекания процесса различают два ее типа: химическую и электрохимическую. Химическая коррозия протекает в средах, не проводящих электрический ток, например, при высокотемпературном нагреве стали для горячей обработки давлением или термической обработки. При этом на поверхности металла образуются различные химические соединения – оксиды, сульфиды и другие – в виде пленки.
В отдельных случаях образовавшиеся при химической коррозии пленки, особенно сплошные, предохраняют металл от дальнейшей коррозии. Например, алюминий, олово, свинец, никель и хром способны к образованию на поверхности металлов плотных защитных пленок. пленки же на стали и чугуне непрочны, способны к растрескиванию и проникновению коррозии вглубь металла.
Электрохимическая коррозия обычно сопровождается протеканием электрического тока. Примерами могут служить ржавление металлических конструкций и изделий в атмосфере, корпусов судов и стальной арматуры гидросооружений в речной и морской воде и т.п.
Детальное рассмотрение механизмов химической и электрохимической коррозии показывает, что резкого различия между ними не существует. В ряде случаев возможен постепенный переход химической коррозии в электрохимическую и, наоборот, механизм коррозии металлов в растворах электролитов может иметь двоякий характер.
Коррозия по условиям протекания бывает следующая. Газовая – коррозия металла в газах при высоких температурах. Коррозия в неэлектролитах (например, коррозия стали в бензине). Атмосферная коррозия различных металлических конструкций на воздухе. Коррозия в электролитах – в проводящих электрический ток жидких средах. Почвенная (например, коррозия подземных трубопроводов). Коррозия внешним током или электрокоррозия (например, повреждение подземной трубы блуждающими токами). Контактная – электрохимическое разрушение металлов, происходящее в результате контакта различных металлов в электролите (например, коррозия деталей из алюминиевых сплавов, соприкасающихся с деталями из меди). Структурная – связанная со структурной неоднородностью металлов; например, ускорение коррозионного процесса чугуна в растворе серной кислоты в результате имеющихся в нем включений графита. Коррозия под напряжением, изменяющимся по значению и знаку, что часто вызывает понижение предела выносливости металла. Коррозия при трении; например, разрушение шейки вала при вращении в морской воде. Щелевая, протекающая в узких щелях и зазорах между отдельными деталями. Биокоррозия – коррозия металлов под воздействием продуктов, выделяемых микроорганизмами, и пота рук человека. По характеру коррозионных процессов и месту их распределения различают сплошную, местную и межкристаллитную коррозию. Сплошная характеризуется тем, что металлическое изделие разрушается почти равномерно и коррозия охватывает всю его поверхность. Сравнительно легко поддается контролю и оценке.
Местная коррозия обычно бывает сосредоточенна на отдельных участках поверхности изделия. Это более опасный вид коррозии, так как распространяется на значительную глубину, а следовательно, приводит к потере работоспособности изделий. Чаще всего этот вид коррозии наблюдается в местах механических повреждений поверхности изделий. При межкристаллитной коррозии процесс разрушения начинается с поверхности изделия и распространяется вглубь его, в основном по границам зерен, что вызывает хрупкость металла и значительное снижение его несущей способности. Этот часто встречающийся на практике вид коррозии является весьма опасным и обычно имеет место при термической обработке металлов или сварке. Степень коррозийной стойкости сталей существенно зависит от содержания углерода. Так, с уменьшением содержания углерода в легированной хромоникелевой стали марки Х18Н9 до 0.015% практически устраняется склонность ее к межкристаллитной коррозии.
Возможно ли устранить следы появления электрохимической коррозии?
К сожалению, не существует стопроцентного метода защиты от коррозии, по крайней мере, экономически обоснованного. Любое изделие рано или поздно подвергнется старению, и избавиться от него будет сложно. Если изделие начало покрываться ржавчиной, в первую очередь следует определить причину.
В быту чаще всего встречается атмосферная коррозия, а способ ее устранения – нанесение неметаллических компонентов, или проще говоря, окрашивание. Однако и тут есть свои нюансы, так как если не устранить следы коррозии, она продолжит распространяться и под покрытием, сведя все старания к нулю.
Для начала необходимо устранить источник заражения. В большинстве это поверхностные очаги, которые удаляются механическим путем, то есть зачисткой. Сложности возникают с очагами глубокого проникновения, когда нет возможности снять такой слой, чтобы устранить дефект
Также особое внимание следует уделить устранению оксидной пленки с поверхности. Она является тем самым электролитом
А простой способ – это обезжиривание. Применяются любые средства с октановым числом: бензин, растворитель и так далее. Не стоит пренебрегать этим процессом, так как если на окрашенной поверхности останется пленка, разрушение продолжится даже под слоем эмали или полимера.
А еще лучше — обратиться к инженеру-проектировщику УК. Он подскажет корень проблемы и поможет с ее решением.
Способы защиты металлов от коррозии
Предотвращение начала или активного протекания коррозии – более удачный способ избавиться от проблем с разрушением металлов, чем постоянная замена или восстановление деталей. Поэтому все производители металлических изделий уделяют максимум внимания разработке и совершенствованию способов защиты своей продукции от ржавления.
На данный момент есть четыре основных направления:
- изменение свойств металла введением добавок. По этому принципу изготавливаются нержавеющие стали – добавки хрома (12%) повышают стойкость сплава к коррозии до почти полной невосприимчивости в нормальных бытовых условиях. Изменения температуры и состава окружающей среды снижают стойкость нержавеющей стали к коррозии;
- использование защитных покрытий. Применяются различные (в чистом виде и комбинациях) лако-красочные, эмалевые, полимерные составы. Также – и с большим успехом – используется поверхностное нанесение менее активных химически металлов (оцинковывание, хромирование, никелирование, золочение);
- применение небольших элементов (пластинок, заклепок) из более активных металлов для сохранения основного объема и массы изделия – коррозии в этом случае подвергаются именно добавленные элементы. Отдельно можно выделить создание слабого тока в самом изделии для нейтрализации тока электрохимической коррозии. Применение этого способа ограничено определенными условиями эксплуатации;
- введение ингибиторов – веществ, угнетающих процесс коррозии – в окружающую изделие среду.
Последний метод требует отдельного рассмотрения.
Виды коррозии
Коррозией называют разрушение металла, находящегося в земле, вследствие электрохимических процессов взаимодействия этого металла с окружающей средой. Иногда к этим воздействиям прибавляются еще быстроменяющиеся по направлению и величине механические напряжения (вибрация), возникающие в оболочках кабелей, проложенных по мостам, вблизи железнодорожного полотна и т. п.
Различают следующие виды коррозии:
Почвенная коррозия
Почвенная коррозия — это электрохимическое разрушение подземных металлических сооружений, вызванное действием окружающей коррозийной среды — грунтов, грунтовых или других вод. При почвенной коррозии разрушение происходит на значительной части поверхности свинцовой оболочки кабеля. В оболочке кабеля образуются пятна, превращающиеся в дальнейшем в углубления. Иногда встречаются повреждения в виде искривленных бороздок вдоль оболочек кабеля.
Электрокоррозия
Электрокоррозия, или коррозия блуждающими токами,— это электрохимическое разрушение металлов, вызванное блуждающими токами в грунте. Блуждающие токи возникают от электрифицированных железных дорог постоянного тока, трамвая и метро. Часть тока ответвляется с рельсов в землю, а также при питании усилителей и линий передач постоянного тока по системе провод — земля. При электрокоррозии происходит разрушение свинцовых оболочек кабеля, выражающееся в образовании отдельных углублений с крутыми стенками или длинных бороздок, расположенных вдоль поверхности кабеля и появления сквозных отверстий.
Межкристаллитная коррозия
Межкристаллитной коррозией называют разрушение, происходящее по границам кристаллов металла, возникающее вследствие постоянных или переменных механических напряжений (вибрации) и действия окружающей коррозийной среды (почвы). При межкристаллитной коррозии образуются мелкие трещины в свинцовой оболочке кабеля, которые приводят к распаду участков оболочки на кусочки.
В условиях эксплуатации могут действовать одновременно все три вида коррозии.
Действие почвенной коррозии или коррозии блуждающими токами вдоль кабеля образует анодные (опасные) и катодные зоны. В катодных зонах токи втекают в оболочки, а в анодных вытекают из них, разрушая металлическую оболочку кабеля. Ток величиной 1 А, стекая со свинцовой оболочки кабеля, способен разрушить в течение года 35— 36 кг свинца, а стекая с брони,— 6—10 кг стали.
Примечания
- Антикоррозионная защита / Козлов Д.Ю.. — Екатеринбург: ООО «ИД «Оригами», 2013. — С. 343. — 440 с. — 1000 экз. — ISBN 978-5-904137-05-2.
- «ГОСТ 5272-68: Коррозия металлов. Термины.»
- Спиридонов А. А. В служеньи ремеслу и музам. — 2-е изд. — М.: Металлургия, 1989. — С. 53. — (Научно-популярная библиотека школьника). — 50 000 экз. — ISBN 5-229-00355-3.
- Merchant and Navy Ship events (1946—2000) — 25/12 1967
- См. также, например, газеты «Ogden Standard Examiner», «Bridgeport Post» за 24 декабря 1967 года.
- ISO 8501-1. «Подготовка стальной основы перед нанесением красок и подобных покрытий. Визуальная оценка чистоты поверхности Часть 1. Степени окисления и степени подготовки непокрытой стальной основы и стальной основы после полного удаления прежних покрытий.»
- Газотермическое напыление
- ГОСТ Р 9.316-2006 «Единая система защиты от коррозии и старения. Покрытия термодиффузионные цинковые. Общие требования и методы контроля.
- Доклад на 16-м Всемирном конгрессе по коррозии в Пекине, сентябрь 2005 года.
- «Руководство для подготовки инспекторов по визуальному и измерительному контролю качества окрасочных работ» — Екатеринбург: ООО «ИД «Оригами», 2009—202 с., ISBN 978-5-9901098-1-5
- «Part Of Bridge On Route I-95 Falls Into River In Greenwich,; Killing 3.». New York Times. June 29, 1983. (англ.)
- (Июнь 2008) «ИЗ ИСТОРИИ КОРРОЗИИ». журнал «Очистка. Окраска»№ 4 (15) : 48. Проверено 2010-10-03.
Местная щелевая коррозия в хлоридсодержащих средах
В жидкостной или газовой системе щели имеются между опорами или хомутами и трубками, между соседними трубопроводами, а также под слоем грязи и отложений, которые могут скапливаться на поверхностях. Избежать образования щелей в трубопроводных конструкциях практически невозможно, и узкие щели представляют собой наибольшую опасность с точки зрения образования коррозии.
Причины образования
Подобно точечной коррозии щелевая коррозия образуется при нарушении пассивированного оксидного слоя, защищающего металл. В результате такого нарушения образуются небольшие точечные очаги. Точечные очаги коррозии разрастаются и углубляются, пока не распространятся по всей щели.
В некоторых местах в стенках трубок могут возникнуть сквозные отверстия. Щелевая коррозия происходит при значительно более низких температурах, чем точечная коррозия.
Материал имеет значение
При проникновении морской воды в трещину некоторая часть ионов железа (Fe++) растворяется и не может быстро покинуть трещину. В соленой воде имеющие отрицательный заряд ионы хлора (Cl-) притягиваются к этим положительно заряженным ионам железа Fe++ и также проникают в трещину. По мере увеличения концентрации хлорида раствор в трещине становится все более коррозионно-активным, что ведет к растворению еще большего количества железа, в результате чего в трещину под воздействием молекулярного притяжения проникает еще больше ионов хлора. В итоге раствор в трещине становится более концентрированным, с высоким содержанием хлорида, который является сильной коррозионной средой.
Способы защиты металлов от коррозии
Предотвращение начала или активного протекания коррозии – более удачный способ избавиться от проблем с разрушением металлов, чем постоянная замена или восстановление деталей. Поэтому все производители металлических изделий уделяют максимум внимания разработке и совершенствованию способов защиты своей продукции от ржавления.
На данный момент есть четыре основных направления:
- изменение свойств металла введением добавок. По этому принципу изготавливаются нержавеющие стали – добавки хрома (12%) повышают стойкость сплава к коррозии до почти полной невосприимчивости в нормальных бытовых условиях. Изменения температуры и состава окружающей среды снижают стойкость нержавеющей стали к коррозии;
- использование защитных покрытий. Применяются различные (в чистом виде и комбинациях) лако-красочные, эмалевые, полимерные составы. Также – и с большим успехом – используется поверхностное нанесение менее активных химически металлов (оцинковывание, хромирование, никелирование, золочение);
- применение небольших элементов (пластинок, заклепок) из более активных металлов для сохранения основного объема и массы изделия – коррозии в этом случае подвергаются именно добавленные элементы. Отдельно можно выделить создание слабого тока в самом изделии для нейтрализации тока электрохимической коррозии. Применение этого способа ограничено определенными условиями эксплуатации;
- введение ингибиторов – веществ, угнетающих процесс коррозии – в окружающую изделие среду.
Последний метод требует отдельного рассмотрения.
Электрохимическая коррозия металлов
Электрохимическая коррозия металлов – это процесс разрушения металлов в среде различных электролитов, который сопровождается возникновением внутри системы электрического тока.
При таком типе коррозии атом удаляется из кристаллической решетки результате двух сопряженных процессов:
- Анодного – металл в виде ионов переходит в раствор.
- Катодного – образовавшиеся при анодном процессе электроны, связываются деполяризатором (вещество — окислитель).
Сам процесс отвода электронов с катодных участков называется деполяризацией, а вещества способствующие отводу – деполяризаторами.
Наибольшее распространение имеет коррозия металлов с водородной и кислородной деполяризацией.
Водородная деполяризация осуществляется на катоде при электрохимической коррозии в кислой среде
2H + +2e — = H2разряд водородных ионов
Кислородная деполяризация осуществляется на катоде при электрохимической коррозии в нейтральной среде
O2 + 4H + +4e — = H2O восстановление растворенного кислорода
Все металлы, по их отношению к электрохимической коррозии, можно разбить на 4 группы, которые определяются величинами их стандартных электродных потенциалов:
- Активные металлы (высокая термодинамическая нестабильность) – это все металлы, находящиеся в интервале щелочные металлы — кадмий (Е 0 = -0,4 В). Их коррозия возможна даже в нейтральных водных средах, в которых отсутствуют кислород или другие окислители.
- Металлы средней активности (термодинамическая нестабильность) – располагаются между кадмием и водородом (Е 0 = 0,0 В). В нейтральных средах, в отсутствии кислорода, не корродируют, но подвергаются коррозии в кислых средах.
- Малоактивные металлы (промежуточная термодинамическая стабильность) – находятся между водородом и родием (Е 0 = +0,8 В). Они устойчивы к коррозии в нейтральных и кислых средах, в которых отсутствует кислород или другие окислители.
- Благородные металлы (высокая термодинамическая стабильность) – золото, платина, иридий, палладий. Могут подвергаться коррозии лишь в кислых средах при наличии в них сильных окислителей.
Электрохимическая коррозия может протекать в различных средах. В зависимости от характера среды выделяют следующие виды электрохимической коррозии:
- Коррозия в растворах электролитов — в растворах кислот, оснований, солей, в природной воде.
- Атмосферная коррозия – в атмосферных условиях и в среде любого влажного газа. Это самый распространенный вид коррозии.
Например, при взаимодействии железа с компонентами окружающей среды, некоторые его участки служат анодом, где происходит окисление железа, а другие – катодом, где происходит восстановление кислорода:
А: Fe – 2e — = Fe 2+
Катодом является та поверхность, где больше приток кислорода.
- Почвенная коррозия – в зависимости от состава почв, а также ее аэрации, коррозия может протекать более или менее интенсивно. Кислые почвы наиболее агрессивны, а песчаные – наименее.
- Аэрационная коррозия — возникает при неравномерном доступе воздуха к различным частям материала.
- Морская коррозия – протекает в морской воде, в связи с наличием в ней растворенных солей, газов и органических веществ.
- Биокоррозия – возникает в результате жизнедеятельности бактерий и других организмов, вырабатывающих такие газы как CO2, H2S и др., способствующие коррозии металла.
- Электрокоррозия – происходит под действием блуждающих токов на подземных сооружениях, в результате работ электрических железных дорог, трамвайных линий и других агрегатов.
Фреттинг-коррозия

Фреттинг-коррозия — коррозионное разрушение на границе двух тел, контактирующих друг с другом, чьи поверхности, находясь под воздействием коррозионной среды, двигаются (скользят) относительно друг друга.
Иными словами, фреттинг-коррозия представляет собой совмещение механического износа (прижатые друг к другу детали, на которые воздействуют колебательные, вращательные, вибрационные напряжения) и воздействия коррозионно-активной среды. Чаще всего скольжение имеет колебательный характер, а объекты испытывают достаточно большую дополнительную нагрузку. Фреттинг-коррозия может наблюдаться при контакте двух металлических материалов, либо же металла и неметалла (резины, пластмассы, которые могут служить прокладочным материалом). Фреттинг-коррозии подвергаются болтовые, шпоночные, заклепочные, шлицевые соединения, контактирующие части подшипников, металлический канат, соприкасающиеся движущиеся валы и многое другое.
Схема возникновения фреттинг-коррозии:
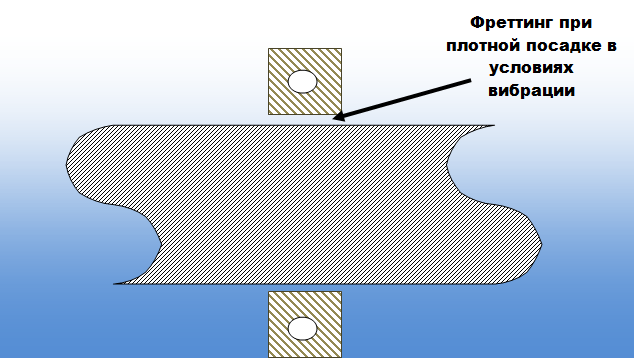
Скорость фреттинг-коррозии зависит от природы используемых металлов (материалов), температуры, состава коррозионной среды и действующих нагрузок. Во время трения происходит нагрев металла, что дополнительно усиливает фреттинг- коррозию, особенно при отсутствии на поверхности смазки.
Способы защитить металл от коррозии
Антикоррозийная защита может проводиться такими методами как:
- Повышение общей коррозионной устойчивости металла методом изменения его хим. структуры;
- Также может использоваться изолирование поверхности металла с применением особенных покрытий;
- Снижение показателя агрессивности места, где применяется металл;
- Применение токов, увеличивающих устойчивость к влиянию коррозии.
Защитные составы достаточно легки в применении, недорого стоят и быстро обновляются при желании, а также создают более декоративный вид для металлического изделия.
Протекция от коррозии обусловливается физической изоляцией металла, или мощным электрическим-химическим влиянием антикоррозионного покрытия на поверхности. Главными минусами большей части лакокрасочных материалов является их слабая водопроницаемость, а иногда и слабая температурная устойчивость.
Защитная пленка как преграда разрушению
Покрытие верхней части металла особым лакокрасочным слоем служит отличной преградой для образования коррозии, а следовательно, способно снижать распространение коррозии. Особое значение в этом деле имеет качество покрытия(используется антикоррозийная краска) – учитывается толщина слоя краски и его пористость.
Также качество покрытия металла будет зависеть от уровня подготовки поверхности и метода работы с антикоррозионным покрытием. Любая ржавчина должны быть зачищена.
Антикоррозионные краски и лаки
Антикоррозийная краска по металлу представляют собой вещество, предохраняющее металл от воздействия опасной внешней среды.
- Составом смазывают поврежденную поверхность.
- Такой материал создает более устойчивое к атмосферному влиянию покрытие.
- Максимальная укрывистость к ржавчине.
Также может использоваться краска по ржавчине. Краска по ржавчине при ее своевременном и правильном нанесении на металл гарантирует долгую протекцию трубопроводов и металлических систем. Такая краска способна защитить элементы механизмов и промышленных аппаратов, а также деталей машин от пагубного влияния ржавчины. С помощью краски проводится обработка технологическим систем и прочего оборудования, в том числе гидротехнических механизмов и мостов.
- Элакор-ПУ — эмали для обработки металлических деталей и краска по металлу.
- Толстослойное антикоррозионное покрытие на основе алкидных смол. FEIDAL Coatings.
- Эмаль ПФ, ПФ 115 и эмаль ПФ-1189. «Сигма краски».
- Антикоррозийная краска NOR-MAALI. Применяется в качестве поверхностной краски. Производитель CARBOLINE — Норвегия, Линейка красок Nor-Maali достаточно широкая – около сотни видов. В основном они используются в промышленных целях: судостроении, мостостроении, строительстве
Однако не любая краска может гарантировать лучший показатель защиты. Стоит рассмотреть виды противокоррозийных эмалей. Специалисты используют ЛКМ для снижения цены работ. Кроме этого, данная продукция ускоряет технологический процесс нанесения покрытия.

































