Контроль качества выполненных работ
Применяемые методы защиты от коррозии металлов подвергаются контролю качества. Выполняется с целью проверки ранее выполненного производственного контроля. Предупреждение дефектов. Разработка мер по устранению обнаруженных дефектов. Контроль качества антикоррозионных работ начинается с проверки документации. Должны быть предоставлена документация на объект антикоррозионной защиты, на применяемые материалы, сертификаты о качестве продукции. По окончании проведения контроля качества работ составляется акт содержащий сведения о месте проведения работ, о состояния проведенных работ, о примененных материалах их марки и расходе. Сведения о организации исполнителе, и подписи лиц проводивших работы. Комиссия, проводящая контроль качества работ проверяет следующие параметры:
— вид антикоррозионного покрытия, не должно быть наличие мест не подвергнутых обработке.
— проверяется толщина слоя покрытия путем замера в различных местах, где предположительно возможна не качественная обработка.
— контролируется адгезия лакокрасочного материала с металлической поверхностью.
Способы защиты от коррозии металлов
Используется несколько основных методов по защите металлических конструкций от разрушительного воздействия коррозии. При использовании защиты в основном делается упор на то, что ржавчина без внешних повреждений не может проникнуть к металлу.
При этом важно, что защитные покрытия выполняют не только предохраняющую функцию, но и придают металлическим конструкциям симпатичный внешний вид. Прежде всего, это покрытия, которые разделяются на три типа, по материалам нанесения:
Прежде всего, это покрытия, которые разделяются на три типа, по материалам нанесения:
- Металлические.
- Неметаллические.
- Химические.
Каждый из них имеет свои особенности и преимущества.
Металлические покрытия. Это способ, при котором на металлическую конструкцию наносят тонким слоем другой вид металла, который более стабилен к разрушительному действию коррозии при аналогичных условиях.
Покрытие может называться анодным или катодным в зависимости от того более активный или менее активный металл сверху.
Неметаллические покрытия. Они подразделяются на органические и неорганические. Чаще всего используется высокополимерный пластик, стекло и керамика. Из органических известны и популярны лаки, битум, краски, а также резина.
Химические покрытия. Это вариант, при котором на поверхности металлической конструкции при помощи химической обработки, наносится пленка, устойчивая к воздействию коррозии. Таких пленок может быть несколько разновидностей:
- Оксидирование — нанесение оксидных пленок.
- Фосфатирование — получение пленки фосфатов.
- Азотирование — пленка из активного азота.
- Воронение стали.
- Цементация — соединение с углеродом.
Также в качестве защиты используется изменение состава коррозийной среды. Еще один вариант защиты — ввести в металл технические соединения, которые повышают стойкость материала к разрушительным действиям коррозии.
Протекторный вид — вариант электрохимической защиты, при которой к конструкции присоединяются пластины с более активным металлом. При этом протектор — материал с отрицательными параметрами потенциала, а защищаемый материал — катод.
Характеристики коррозии

Коррозия в простонародии больше известная под названием ржавчина. Она представляет собой процесс самопроизвольного образования на металлической поверхности налета в результате влияния окружающей среды. Ржавчина обычно имеет темно-коричневый оттенок, который портит внешние качества изделия из того или иного металла.
Коррозия металла сегодня встречается достаточно часто. Причиной ее появления является то, что некоторые виды металлических материалов являются неустойчивыми к температурным перепадам и изменениям влажности. Изделиям из металлов достаточно часто приходится контактировать с различными веществами. Они могут влиять на них по-разному. В результате образуется коррозия различных видов.
В результате конструкция, которая из него создана, приходит в негодность.
Коррозии подвергаются не только металлы, но и другие материалы. Сегодня довольно часто встречаются случаи, когда она появляется на пластмассе. Образование ржавчины присуще и бетонным изделиям.
Скорость коррозии зависит от размера температуры. С повышением температуры на каждые сто градусов появление ржавчины становится быстрее.
https://youtube.com/watch?v=KB4Qq92zKK0
Органосиликатные покрытия
Для качественной защиты от коррозии рекомендуется применение металлов с высоким уровнем гидрофобности, непроницаемости в водных, газовых и паровых средах. К числу таких материалов относятся органосиликаты.

Химическая коррозия практически не распространяется на органосиликатные материалы. Причины этого кроются в повышенной химической устойчивости таких композиций, их стойкости к свету, гидрофобных качествах и невысоком водопоглощении. Также органосиликаты устойчивы к низким температурам, обладают хорошими адгезивными свойствами и износостойкостью.
Проблемы разрушения металлов из-за воздействия коррозии не исчезают, несмотря на развитие технологий борьбы с ними. Причина в постоянном возрастании объемов производства металлов и все более сложных условий эксплуатации изделий из них. Окончательно решить проблему на данном этапе нельзя, поэтому усилия ученых сосредоточены на поисках возможностей по замедлению коррозионных процессов.
Рекомендации
Советы:
- На защите деталей лучше не экономить, и покрыть их резиновой или полимерной краской.
- Перед использованием абразивов нужно попробовать удалить ржавчину щадящими составами.
- Сложные коррозионные процессы можно останавливать с помощью агрессивных химикатов, но прежде чем их использовать, нужно изучить свойства состава, характеристики металла, чтобы предотвратить возможные негативные реакции.
Коррозионные процессы могут быстро разрушить любой материал. Порча металлоконструкций в некоторых ситуациях может иметь катастрофические последствия. Изучив способы защиты от образования коррозии, нужно применить один из наиболее подходящих.
Атмосферная коррозия алюминия
Рисунок 1.1 – Атмосферная (общая) коррозия алюминия
Факторы атмосферной коррозии
Сопротивление алюминия и его сплавов атмосферной коррозии зависит:
1) от климатических условий, в которых они находятся:
- влажности;
- продолжительности и интенсивности дождей;
- температуры;
- количества солнечных дней в году;
2) от степени загрязнения воздуха, то есть концентрации:
- диоксида серы (SO2);
- оксидов азота (NOx);
- количества и химического состава пыли.
Климатические факторы и степень загрязненности атмосферы действуют совместно. Например, повешенная загрязненность воздуха может снижать критическую величину относительной влажности воздуха, при которой начинает развиваться коррозия. Эти факторы могут также давать противоположные результаты: дождь повышает влажность воздуха, но также смывает пыль и продукты коррозии, что может снижать скорость коррозии
Относительная влажность
Скорость атмосферной коррозии зависит от относительной влажности воздуха, а не просто от количества или интенсивности дождей в данной местности. Дождь является одним, но не единственным фактором, от которого зависит относительная влажность воздуха.
Уровень относительной влажности – это отношение между фактическим давлением водяного пара и максимальным давлением водяного пара при данной температуре. Это отношение выражается в процентах.
При нормальной комнатной температуре воздух считается:
- сухим, если относительная влажность составляет не более 30 %;
- нормальным, если относительная влажность находится в пределах от 50 до 60 %;
- влажным, если относительная влажность выше 80 %;
- насыщенным влагой, если относительная влажность около 100 %.
В пустынях и засушливых зонах уровень относительной влажности редко превышает 10-20 %, тогда как в умеренном климате он находится в основном между 40 и 60 %. Во время ливня она может достигать 90-95 %, а во время тропических дождей приближаться к 100 % .
Точка росы
Точкой росы называется температура, при которой будет начинаться конденсация влаги. Для данного уровня относительной влажности это та температура, до которой нужно охладить воздух, чтобы он стал насыщенным влагой, и началось ее выпадение на ближайших поверхностях.
Длительность увлажнения и сульфатный электролит
Коррозия металлов на открытом воздухе зависит от так называемой длительности увлажнения и химического состава поверхностных электролитов. Длительностью увлажнения называется период, в течение которого на поверхности металла достаточно влаги для возникновения коррозии. Длительность увлажнения обычно определяют, как время, в течение которого относительная влажность воздуха превышает 80 % и, в тоже время, температура на поверхности металла составляет выше 0 ºС. При этих условиях на поверхности металла может возникать конденсация влаги.
Критическая относительная влажность
Атмосферная коррозия металлов, в том числе, алюминия, происходит в тонких пленках влаги, которые расположены на поверхности металла. Существует критический порог относительной влажности, ниже которого алюминий и его сплавы не подвергаются коррозии. Это происходит потому, что при недостаточной влажности не хватает влаги, чтобы создать непрерывную электролитическую пленку на поверхности металла. Для свежее обработанной поверхности алюминия в не загрязненной атмосфере этот порог составляет около 66 % (рисунок 1.2) .
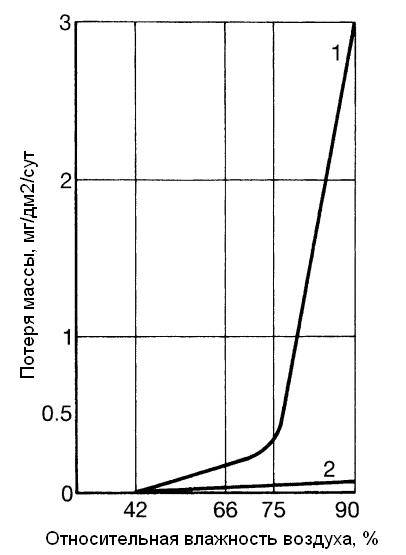 Рисунок 1.2 – Влияние влаги на атмосферную коррозию алюминия : кривая 1 – с концентрацией SO2 около 1 %; кривая 2 – без SO2
Рисунок 1.2 – Влияние влаги на атмосферную коррозию алюминия : кривая 1 – с концентрацией SO2 около 1 %; кривая 2 – без SO2
Нет сульфатов – нет коррозии
В нормальных сельских районах и в атмосферах с умеренной степенью загрязненности сульфатами, стойкость алюминия к воздействию окружающей среды очень высокая. В атмосфере с высоким содержанием сульфатов и высокой влажностью на алюминиевых изделиях может возникать точечная (язвенная) коррозия. В таких условиях алюминий может потребовать коррозионной защиты.
Хлориды
Присутствие в воздухе солей (особенно хлоридов) снижает долговечность алюминия, но в меньшей степени, чем для большинства других строительных материалов. Максимальная глубина ямок коррозии составляет обычно только незначительную часть толщины алюминиевой детали. В отличие от углеродистой стали прочностные свойства алюминиевых деталей, подвергшихся коррозии, остаются практически неизменными.
Как корродирует металл
Ущерб, наносимый коррозией памятникам заметен всем. Уже побывали на реставрации “Рабочий и колхозница”, установленные на ВДНХ, кони Клодта с Аничкова моста, американская статуя Свободы. И на восстановление их внешнего вида тратятся огромные деньги.
Иногда разрушение не идет дальше поверхности — металл покрывается оксидной пленкой, которая предохраняет его от дальнейшего проникновения агрессора — воздуха и влаги. Так зеленеет медь, бронза. Иногда металл рассыпается как труха — так ржавеет железо.
А вот что происходит с металлами, которые используют для покрытия домов. Возьмем оцинкованную железную крышу. Потери цинка в год в сельской атмосфере оцениваются в 7-15 г на кв. м, а в городской — в 43 г на кв. м.
Сталь коррозирует еще быстрее: в сельской атмосфере теряется до 430 г на кв. м, в городской — до 600 г. Больше полкилограмма стали в год на один квадратный метр!
Особенности антикоррозионных составов
 В местах скола краски видна ржавчина, а на осях покрытых смазкой коррозии нет
В местах скола краски видна ржавчина, а на осях покрытых смазкой коррозии нет
Что такое ингибиторы коррозии? Это такие вещества и элементы, которые, присутствуя в среде, подверженной опасному влиянию коррозии, в состоянии уменьшать и в целом останавливать коррозионное воздействие на металл. Ингибитор коррозии может представлять собой как одно химическое соединение, так и быть смесью многих.
Ингибиторами наиболее часто являются ПАВ вещества, а также всевозможная органика. При влиянии на изделие они еще сильнее улучшают защитные характеристики оксидной пленки на металле. По этой причине вы можете сделать вывод, что присутствие кислорода в среде благоприятствует подъему защитного эффекта от воздействия коррозии. Однако, если оксидная пленка имеет слабую устойчивость — ухудшается адсорбция ингибитора на верхнем слое металла.
- Ингибитор солеотложений ИОМС-1 (раствор)г 200 руб/кг. Макрофлекс.
- Ингибитор коррозии Protectogen(протектоген). C Aqua.
- Комплексонат – раствор цинкового комплекса. Эктоскейл.
- ГАЛАН. Протектор. Ингибитор коррозии (5 л). Защищает от коррозии трубопроводы, радиаторы и прочие системы отопления.
Основные типы коррозии
Говоря о механизме коррозийного процесса можно заметить 2 главных типа коррозии: химическую и электрохимическую.
Химическая — это явственный итог прохождения реакций, во время которых, после уничтожения металлической связи, части металла и все атомы, которые входят в окислители, создают собой крепкую связь. Электроток между различными частями поверхности металл не может возникнуть. Данная разновидность коррозии может быть присуща химическим средам, которые не в состоянии передавать электроток. Сюда относятся газы и неэлектролиты.
Важно помнить, что на скорость коррозии влияют также причины коррозии. Электрохимическая коррозия представляет процесс деградации металлов
Этот процесс идет вместе с возникновением в системе электричества.
Классификация коррозии по значению протекания самого процесса
Арка моста, с более сильной ржавчиной с местах где разрушен лакокрасочный слой
Коррозионные процессы могут быть разделены:
- по типу взаимного влияния металлов с окружающей атмосферой;
- по типу коррозионной атмосферы и условиям самого процесса;
- по характеристике дегенерационного воздействия;
- на «скорость коррозии» очень сильно влияет тип окружающей атмосферы.
Электрохимическая коррозия
Предыдущая43Следующая
Электрохимическая коррозия – разрушение металлов в среде электролита.
Детали многих металлических конструкций работают в среде электролита: опоры мостов, водный транспорт, паровые котлы, химическая аппаратура, водопроводные трубы, кузова автомобилей. В сырую погоду, при суточных колебаниях темпертур на поверхности металлов конденсируется пленка воды, в которой растворяются газы из загрязненной атмосферы (СO2, SO2, NO2, H2S, и др.) и образуется электролит.
Поверхность металлов неоднородна. На поверхности металла имеются дефекты кристаллической решетки, примеси других металлов, включения соединений с неметаллами и интерметаллические соединения, продукты взаимодействия с окружающей средой (оксиды, гидроксиды, соли, грязь), неровности поверхности. Эти участки поверхности металла в растворе электролита будут иметь другой, отличный от основного металла потенциал. Таким образом, на поверхности металлов создается система локальных, короткозамкнутых через металл гальванических элементов. Работа этих микроскопических элементов сопровождается коррозионным разрушением металла.
В качестве примера рассмотрим модель гальвано-пары железо-медь в кислой и нейтральной средах. В гальванопаре Fe/Cu более активным является железо, стандартный потенциал которого –0,44 В, а у меди +0,34 В. В кислой среде на аноде будет проходить реакция окисления железа:
Fe0 –2ē → Fe2+.
Ионы железа – Fe2+ – будут переходить в раствор, электроны – на медь, заряжая ее отрицательно. На поверхности меди ионы Н+ из раствора восстанавливаются (водородная деполяризация):
2H+ +2ē → H2.
Суммарная окислительно-восстановительная реакция коррозии железа:
Fe0 + 2H+ → Fe2+ + H2.
В нейтральных и щелочных растворах на катодных участках поверхности металла происходит процесс восстановления растворенного в воде кислорода (кислородная деполяризация):
O2 + 2H2O +4ē → 4OH–.
Суммарная реакция коррозионного процесса:
2Fe0 + O2 + 2H2O → 2Fe2+ + 4OH–, Fe2+ + 2OH– → Fe(OH)2.
В результате коррозии образуется Fe(OH)2, который дальше окисляется атмосферным кислородом воздуха до Fe(OH)3, окончательный продукт окисления – гидратированный оксид железа (III) (ржавчина):
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3 → 4FeOOH + 4H2O.
Рис. 9.4. Схема коррозии в кислой среде при контакте с менее активным металлом.
Гальванические пары возникают также при контакте металла с его химическими соединениями. Например, при коррозии стали анодом является зерна железа, катодом – карбид железа Fe3C (рис. 9.5).
Рис. 9.5. Схема образования коррозионных гальванических микроэлементов в углеродистой стали, находящейся во влажном воздухе
Разность потенциалов может возникнуть вследствие различной концентрации растворенного кислорода. Раствор на поверхности металла и на участках, куда затруднен доступ кислорода, вследствие конструкционных особенностей деталей, содержит разное количество растворенного кислорода, что ведет к возникновению разности потенциалов на этих участках деталей.
В промышленных центрах атмосфера содержит загрязняющие газы: SO2, NO2, CO2, H2S и др., которые растворяясь в воде, дают кислоты, агрессивные по отношению к металлам. В кислой среде на железе будет протекать процесс коррзии с водородной деполяризацией. О влиянии состава атмосферного воздуха на скорость коррозии можно судить по следующим данным: в сельской местности скорость коррозии стали составляет 100-250, в промышленных городах 450-550 г/м2 в год.
В нейтральной среде (при достаточно чистой атмосфере) коррозия протекает с кислородной деполяризацией. Почему же скорость коррозии, прокающей с кислородной поляризацией ниже?
Для того чтобы коррозия имела место необходимо условие – электродный потенциал металла должен быть отрицательнее потенциала окислителя (деполяризатора)
Таблица 9.1
Зависимость потенциала газовых электродов от рН
| pН раствора | Е (2Н+/Н2,Pt), В | Окисляющиеся металлы | Е (О2/2ОН–), В | Окисляющиеся металлы |
| 0,0 | Pb | 1,23 | Hg | |
| –0,414 | Fe | 0,815 | Аg | |
| –0,828 | Щелочные и щ-зем., Zn, Al | 0,401 | Cu |
Как следует из данных приведенных в таблице, большинство металлов могут подвергаться коррозии с кислородной деполяризацией, но процесс этот медленный, т.к. кислород малорастворим в воде, и скорость его подвода к металлу невелика. Поступающий к поверхности металла кислород практически весь сразу же восстанавливается. При этом на поверхности некоторых металлов может образоваться защитная оксидная пленка, некоторые металлы при определенных условиях могут вообще переходить в пассивное состояние.
Предыдущая43Следующая
Дата добавления: 2017-11-21; просмотров: 745;
НАРОДНОХОЗЯЙСТВЕННОЕ ЗНАЧЕНИЕ БОРЬБЫ С КОРРОЗИЕЙ
Потери от коррозии можно разделить на прямые и косвенные. Прямые потери – это стоимость заменяемых изделий, затраты на защитные мероприятия и безвозвратные потери металла вследствие коррозии. По подсчетам специалистов, таковые в мировом масштабе составляют в настоящее время около 10…15% от объема производства стали. Косвенные – потери продукта в результате утечек, снижение производительности агрегата, загрязнение продуктами коррозии целевого продукта и т.п.
Значительная часть мощности предприятий черной металлургии затрачивается на восполнение потерь металла вследствие коррозии. Однако это далеко не полностью отражает действительный ущерб, связанный с выходом из строя изделий из металла. Значительные потери обусловлены авариями оборудования, его простоями, потерями и отходами в металлообработке, нарушениями качества продукции и в конечном счете повышением ее себестоимости и снижением производительности труда. Поэтому экономия металла, повышение качества исходного сырья и металлоизделий, уменьшение коррозионных потерь – непременное условие повышения эффективности производства и качества продукции, которое должно обеспечиваться в государственном масштабе.
Местная щелевая коррозия в хлоридсодержащих средах
В жидкостной или газовой системе щели имеются между опорами или хомутами и трубками, между соседними трубопроводами, а также под слоем грязи и отложений, которые могут скапливаться на поверхностях. Избежать образования щелей в трубопроводных конструкциях практически невозможно, и узкие щели представляют собой наибольшую опасность с точки зрения образования коррозии.
Причины образования
Подобно точечной коррозии щелевая коррозия образуется при нарушении пассивированного оксидного слоя, защищающего металл. В результате такого нарушения образуются небольшие точечные очаги. Точечные очаги коррозии разрастаются и углубляются, пока не распространятся по всей щели.
В некоторых местах в стенках трубок могут возникнуть сквозные отверстия. Щелевая коррозия происходит при значительно более низких температурах, чем точечная коррозия.
Материал имеет значение
При проникновении морской воды в трещину некоторая часть ионов железа (Fe++) растворяется и не может быстро покинуть трещину. В соленой воде имеющие отрицательный заряд ионы хлора (Cl-) притягиваются к этим положительно заряженным ионам железа Fe++ и также проникают в трещину. По мере увеличения концентрации хлорида раствор в трещине становится все более коррозионно-активным, что ведет к растворению еще большего количества железа, в результате чего в трещину под воздействием молекулярного притяжения проникает еще больше ионов хлора. В итоге раствор в трещине становится более концентрированным, с высоким содержанием хлорида, который является сильной коррозионной средой.
Коррозия металлов. Способы борьбы с коррозией
Как организовать дистанционное обучение во время карантина?
Помогает проект «Инфоурок»
Описание презентации по отдельным слайдам:
Определение: Коррозией (от латинского corrodere – разъедать) называют самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды.
Коррозия вызывает серьезные экологические последствия. Утечка газа, нефти и других опасных химических продуктов из разрушенных коррозией трубопроводов приводит к загрязнению окружающей среды.
Коррозию металлов и сплавов (их окисление) вызывают такие компоненты окружающей среды, как вода, кислород, оксиды углерода и серы, содержащиеся в воздухе, водные растворы солей.
Эти компоненты непосредственно окисляют металлы – происходит химическая коррозия. При электрохимической коррозии (наиболее частая форма коррозии) всегда требуется наличие электролита (Конденсат, дождевая вода и т. д.) как, например, при ржавлении железа во влажной атмосфере.
Чаще всего коррозии подвергаются изделия из железа. Особенно корродирует металл во влажном воздухе и воде. Химическое уравнение этого процесса: 4Fe + 3O2 + 6H2O → 4FeO(OH)•H2O
Химически чистое железо почти не корродирует, а техническое железо, которое содержит различные примеси, например в чугунах и сталях, ржавеет. Следовательно, одной из причин возникновения коррозии является неоднородность металла.
Способы борьбы с коррозией: 1. Нанесение защитных покрытий на поверхности предохраняемого от коррозии металла. Для этого используют масляные краски, эмали, лаки. Эти неметаллические покрытия недорогие, но обычно недолговечные.
Способы борьбы с коррозией: Предохраняемый металл можно покрыть слоем другого металла: золота, серебра, хрома, никеля, олова, цинка и др. Один из самых старых способов – лужение – это покрытие железного листа слоем олова. Такое железо называют белой жестью.
Причины возникновения коррозии
Разрушение металлов под воздействием коррозионных процессов вызывается многими причинами. Наибольший вред наносят химические и электрохимические коррозионные процессы. В первом случае в ходе химических реакций образуются соединения металлов с различными агрессивными веществами, присутствующими в окружающей среде. Во втором случае металлы растворяются в электролитах, которые образуются в воздухе или воде.
Кроме того, металлы страдают от коррозии вследствие воздействия радиации и различных микроорганизмов. Механические напряжения ускоряют коррозионные процессы, так как они уменьшают термостойкость металлов, повреждают присутствующие на их поверхности оксидные пленки и способствуют возникновению трещин и неоднородностей.
Существуют следующие виды коррозии:
- местная (затрагивает только отдельные участки поверхности металлов);
- равномерная (охватывает всю поверхность металлов);
- межкристаллитная (проявляется в разрушении металлов по границам зерен).